学院动态
数理学院2023级研究生毛珈琪为第一作者在国际权威期刊《Nature Communications》和《Chemical Communications》发表文章
来源:数理学院 浏览人数: 发布时间:2026-04-14
该课题组在生物大分子液-液相分离(LLPS)领域取得重要研究进展,相关成果分为理解染色质组织及DNA结构动态调控机制提供了新视角。
成果一:揭示病毒RNA基因组的相分离机制

乙肝病毒是导致慢性肝炎、肝硬化和肝癌的主要原因,全球有数亿感染者,并导致每年约80万死亡病例。理解乙肝病毒的分子组装机制对开发抗病毒药物至关重要。乙肝病毒虽为DNA病毒,但在其生命周期早期,其前基因组 RNA(pgRNA)需要与聚合酶一起加载到病毒壳体中。由于RNA带负电且空间极度受限(几十纳米),基因组通常面临巨大的静电排斥力。研究团队通过多尺度计算模拟,并结合单分子和生化实验,发现pgRNA并非均匀地填充在衣壳内,而是利用液液相分离机制,在衣壳内表面凝聚组装成空心的球壳状液态凝聚体(condensates)。这种凝聚体呈现低密度区与高密度区共存的异质性特征。
该研究指出,导致乙肝病毒基因组液液相分离的核心驱动力是衣壳蛋白中高度无序且带正电的C端结构域(CTD)与带负电的pgRNA之间的强静电相互作用。相分离驱动基因组形成了由“有序双链RNA阵列”和“柔性单链链接区”相互交织的微相结构(图1)。这种设计在保持结构有序性的同时,赋予了基因组必要的动态柔性。有趣的是,虽然大量病毒颗粒的平均密度分布符合标准的正二十面体对称性,但在单个病毒颗粒层面,基因组分布表现出明显的异质性和对称性破缺,反映了其液态凝聚体的动态本质。这种由相分离形成的空心球壳结构显著增强了乙肝病毒聚合酶在衣壳内的扩散速率,并促进了远程RNA碱基配对,这是乙肝病毒进行高效逆转录的必要前提。因此,针对乙肝病毒基因组的相行为进行干预,可能成为一种全新的抗病毒策略。
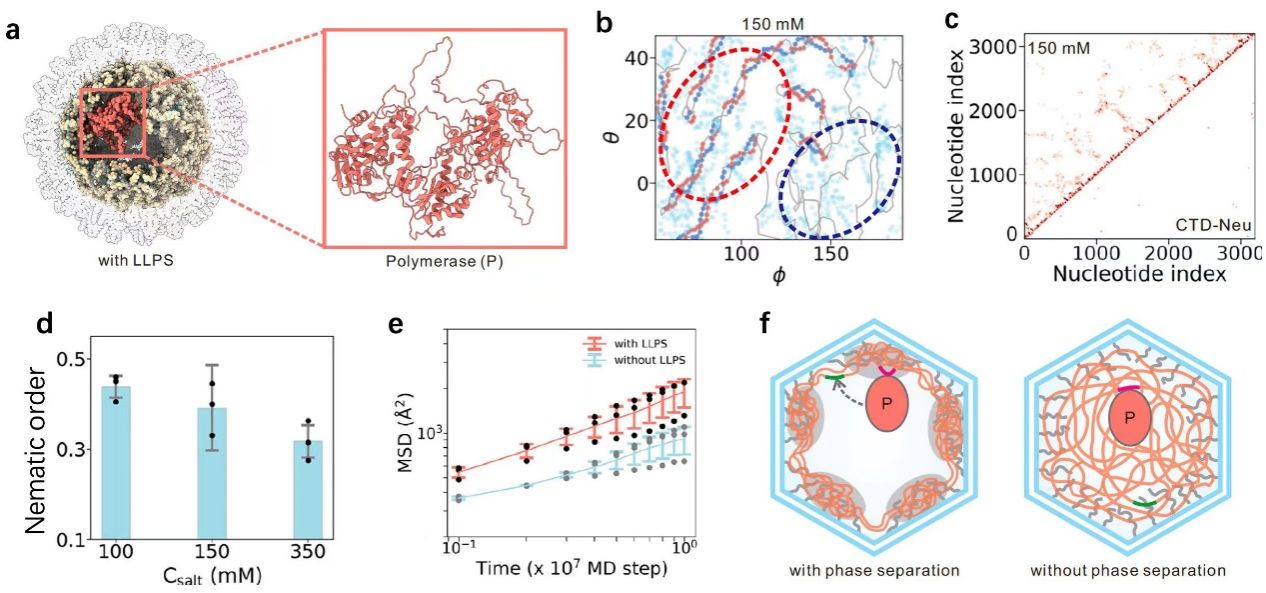
图1. 液液相分离形成的病毒基因组微相结构的结构有序性与动态柔性促进逆转录酶在受限衣壳内的扩散与基因组RNA长程碱基配对,加速乙肝病毒逆转录过程。
成果二:阐明DNA结构动态对相分离的主动调控作用

液-液相分离(Liquid-Liquid Phase Separation,LLPS)是无膜细胞器的核心形成机制,通过将蛋白质和核酸组织成高度动态的凝聚体,精准调控细胞核内的多种生物学功能。传统观点认为,核酸在此过程中主要扮演被动支架的角色。然而,本研究发现,具有特定结构特征的DNA分子相较于无结构DNA,能够更有效地介导组蛋白H1的液-液相分离,提示DNA可能主动参与调控这一过程。研究团队系统比较了多种DNA底物与组蛋白H1的相分离能力,创新性地将单分子荧光共振能量转移(smFRET)技术与显微成像相结合,首次在单分子水平揭示了DNA构象动力学对组蛋白H1介导液-液相分离的主动调控机制。
该研究聚焦DNA同源重组关键中间体——霍利迪连接体(Holliday Junction, HJ),与典型的IDR蛋白——组蛋白H1(Histone H1,H1)的相互作用。通过分析不同DNA类型在离子环境及H1作用下的构象动态与凝聚特性,发现具备结构特征的 DNA 对 H1 介导的液-液相分离具有更强促进作用,其能力呈现 ssDNA< dsDNA < HJS < HJF 的层级趋势(图2),说明 DNA 并非被动支架,其结构与序列特征能够显著影响蛋白质-核酸凝聚体的形成与稳定性。smFRET结果进一步表明,值得注意的是,这一动力学增强效应具有显著的离子依赖性:在低至中等浓度的Na⁺或Mg²⁺条件下效应最为突出;而在高盐环境中,由于静电屏蔽效应及竞争性离子结合,该促进作用明显减弱。该研究揭示了一种可离子调控的分子开关机制,通过HJ-H1的特异性相互作用,将DNA的结构特征与局部生物分子凝聚事件动态关联,为深入理解染色质结构调控、基因转录及DNA损伤修复等关键生物学过程提供了新的理论视角。
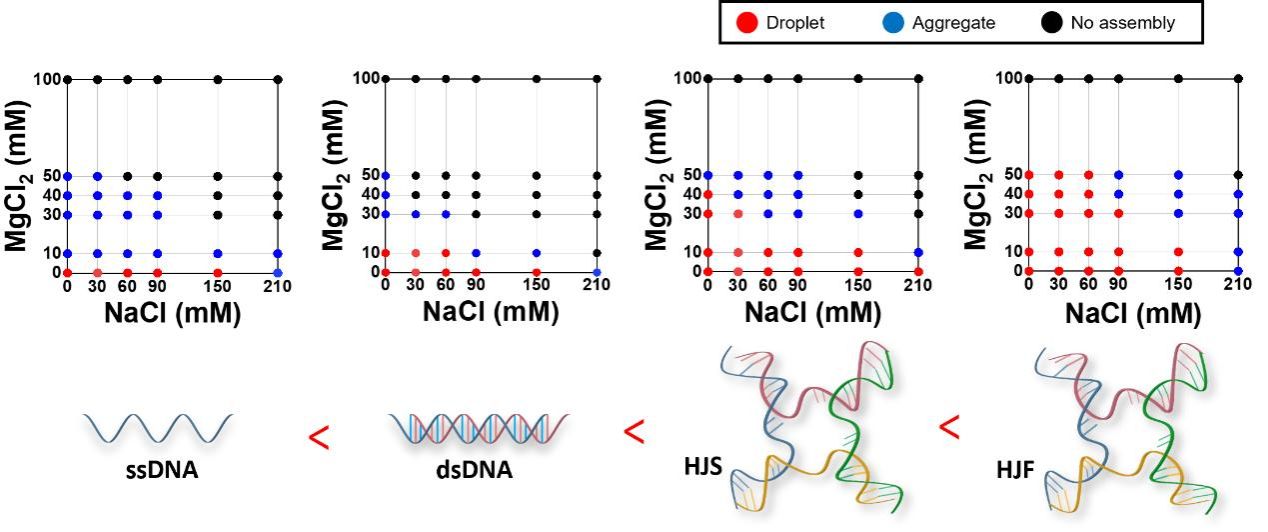
图2. 不同离子条件下组蛋白H1与不同DNA底物的相图。
该系列成果数理学院2023级硕士研究生毛珈琪分别为共同第一作者和唯一第一作者,指导老师及通讯作者为温州大学王艳伟副教授和杨光参教授,论文合作者为国科温州研究院边运强副研究员,潘海副研究员,南京大学生物物理团队王炜教授、李文飞教授、曹毅教授等。该系列工作受到国科温州研究院、江苏省基础研究重点项目、南京鲲鹏/昇腾孵化中心、以及江苏省血管信息与健康工程医学重点实验室支持。感谢国家自然科学基金委员会项目(编号22403019、12574247)以及浙江省自然科学基金项目(LY23A40002)、中国科学院温州研究院启动资金(项目编号WIUCASQD2021007、WIUCASQD2022003)的资助支持。
一审:叶戴茜 二审:陈亮 三审:潘莉莉、王艳伟





